大動脈疾患
- 大動脈瘤
- 大動脈解離
- 大動脈炎
今回は大動脈解離に関して説明します。
- 大動脈解離とは
- 有病率
- リスク因子・原因
- 分類
- 症状
- 検査
- 治療・手術適応
- 合併症
- 予後
治療・手術適応
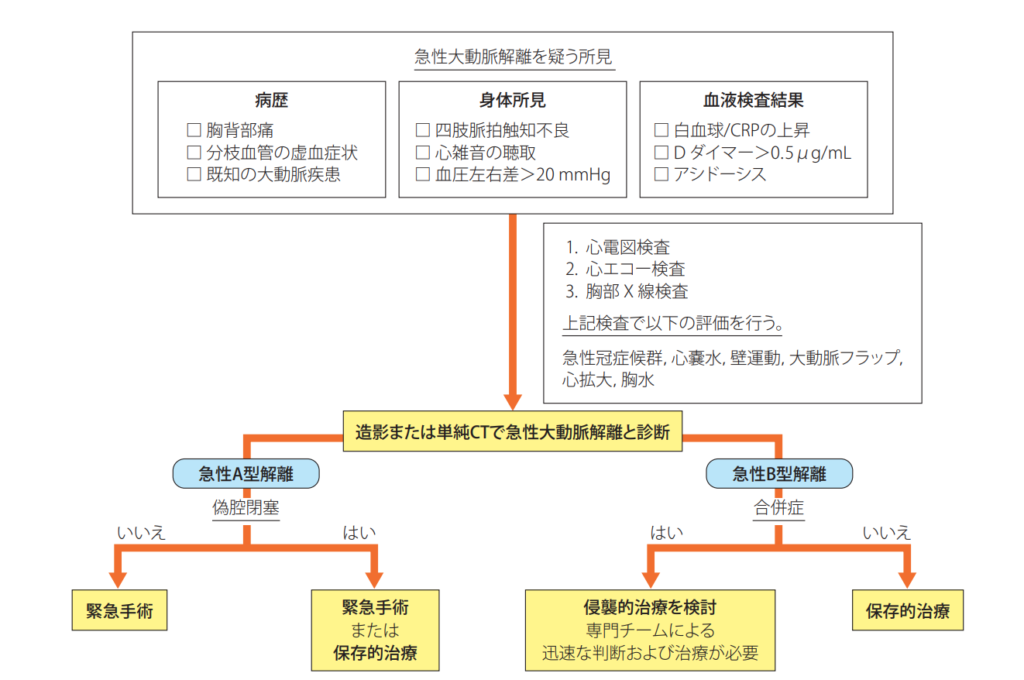
急性大動脈解離はStanfordA型とStanfordB型で治療方針が大きく異なります。
基本的は方針は以下の通りです
- StanfordA型―緊急手術
- StanfordB型―保存的加療、後に手術
StanfordA型でも保存的加療を選択できることも、StanfordB型でも緊急手術の適応になることもあります。
初期治療と並行し、診断も行います。
初期治療
まずは解離腔の進展を抑えるためバイタルサインを確認し、鎮痛と血圧コントロールを行います。
急性大動脈解離は「高血圧によって動脈壁が裂け、非常に強い疼痛を自覚します。その疼痛のためまた血圧が上がり、動脈が裂ける」。この繰り返しです。
そのため、疼痛管理(麻薬も使用します)と血圧コントロールが最も大切です。
逆に血圧低下、ショックの場合は心タンポナーデか大量胸腔内出血を疑います。
- 心タンポナーデー直ちに心膜穿刺、排液を行い、緊急外科手術を行います。
- 胸腔内出血ードレナージが必要ですが、呼吸不全があるときは気管内挿管する。
これらの処置は救急外来でやるよりは手術室で行う方が安全です。
多くの症例で発症直後は血圧が上昇しているため、疼痛管理(麻薬も使用します)と血圧コントロールで収縮期圧を100~120mmHgにします。
急性大動脈解離Stanford A型
急性大動脈解離Stanford A型は極めて予後不良な疾患であり、発症直後の死亡率は1~2%/時間とされ,発症から治療開始までの時間をいかに短縮できるかが重要である。
急性大動脈解離Stanford A型における急性期治療の適応
ClassⅠ
- 偽腔開存型A型解離に対する外科治療(緊急手術)
- 解離に直接関係のある,重症合併症*を持ち,手術によりそれが軽快するか,または,その進行が抑えられると考えられる大動脈解離に対する外科治療
※偽腔の破裂、再解離、心タンポナーデ、脳循環障害、大動脈弁閉鎖不全、心筋梗塞、腸管虚血、四肢血栓塞栓症など
ClassⅡa
- 血圧コントロール,疼痛に対する薬物治療に抵抗性の大動脈解離に対する外科治療
ClassⅠb
- 偽腔閉塞型A型解離に対する外科治療
- 偽腔閉塞型A型解離に対する内科治療
- 上行大動脈の偽腔が血栓閉塞したDeBakeyⅢ型の逆行性解離に対する内科治療
※心タンポナーデのなく、上行大動脈径が50mm以下で血栓化した偽腔の径が11mm以下の症例に限る。
急性大動脈解離Stanford B型
B型解離はA型解離よりも予後が良く、合併症のないB型解離の30日死亡率は10%以下である.外科治療が必要となるのは、
- 合併症(破裂,再解離,灌流異常など)を有する症例
- 疼痛に対する薬物治療に抵抗性のB型解離である。
- 内科的治療下に大動脈径の拡大傾向(≧55mm)を認める症例やULPが新たに出現する症例では破裂の危険性があり手術を考慮する。急性期の最大動脈径>40mmあるいは最大部位が弓部遠位にある症例は遠隔期の予後不良因子とされており注意が必要である。
内科治療の場合、安静度は破裂の可能性の高いとされる48時間以内は,絶対安静である.100~120mmHgで血圧管理を行い、急性大動脈解離のリハビリプログラムに沿ってリハビリを進めます。
急性大動脈解離Stanford B型における急性期治療の適応
ClassⅠ
- 合併症のない偽腔開存型および偽腔閉塞型B型解離に対する内科治療
- 解離に直接関係のある重症合併症*を持ち,手術によりそれが軽快するか,または,その進行が抑えられると考えられる大動脈解離に対する外科治療
※偽腔の破裂、再解離、心タンポナーデ、脳循環障害、大動脈弁閉鎖不全、心筋梗塞、腸管虚血、四肢血栓塞栓症など
ClassⅡa
- 血圧コントロール,疼痛に対する薬物治療に抵抗性の大動脈解離に対する外科治療
- 血圧コントロールに対する薬物治療に抵抗性の大動脈解離に対する内科治療
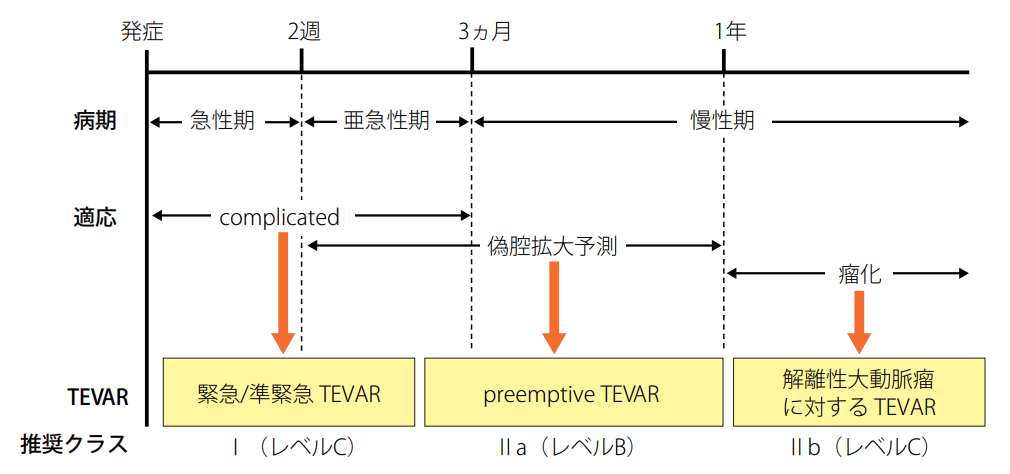
慢性大動脈解離
慢性大動脈解離の管理は血圧コントロールと心拍数コントロールです。
目標値として,安静時130mmHg未満,最大活動時でも150mmHg未満が望ましいです。
また、手術適応は一般的には真性瘤に準じて、胸部大動脈で最大短径60mm,腹部大動脈で50mmあるいは径拡大速度5mm/年以上とされます。
大動脈のremodelingを考えると急性大動脈解離Stanford B型の偽腔開存型であれば保存的加療終了後、発症から3ヶ月頃にエントリー閉鎖をした方が予後改善になるといわれています。
保存的加療・大動脈解離リハビリプログラム
リハビリプログラムは標準コースと短期コースで分かれます。
以下を満たす場合は短期コースを適応します。
- 急性大動脈解離Stanford B型症例
- 破裂,切迫破裂ではない
- malperfusion(分枝灌流障害)がない
- 痛みのコントロールができている
- 血圧,心拍数のコントロールが達成されている (収縮期血圧を100~120 mmHg、心拍数も60回 /min未満)
- 大動脈最大短径4cm以下
- 偽腔閉塞型でのULPなし
- 偽腔開存型での真腔1/4以下の症例
- 大動脈径の拡大(胸部大動脈瘤合併)がない
- DIC(播種性血管内凝固症候群)の合併がない
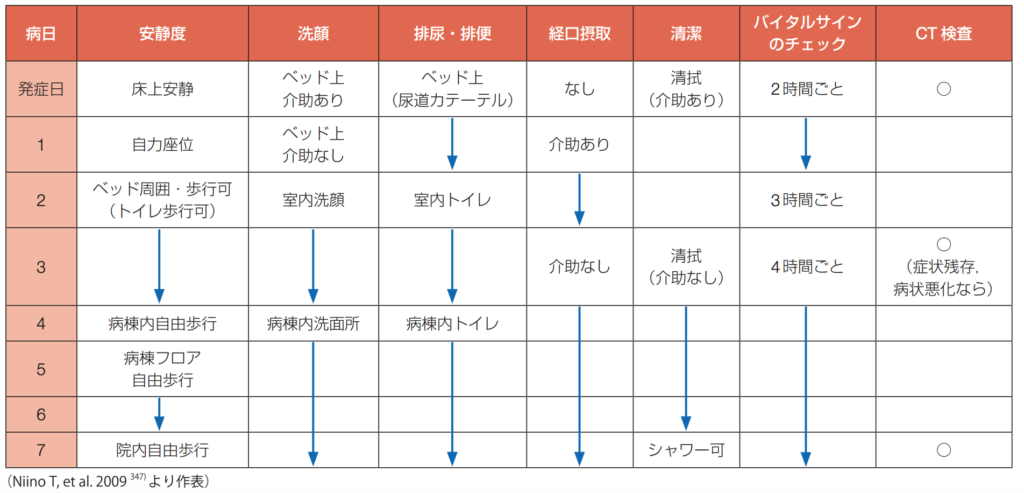
リハビリプログラムの標準コースを下記に示します。
予後
急性大動脈解離では解離した部位により危険性は異なります。
急性大動脈解離Stanford A型とStanford B型の生存率のグラフを下記に示します。
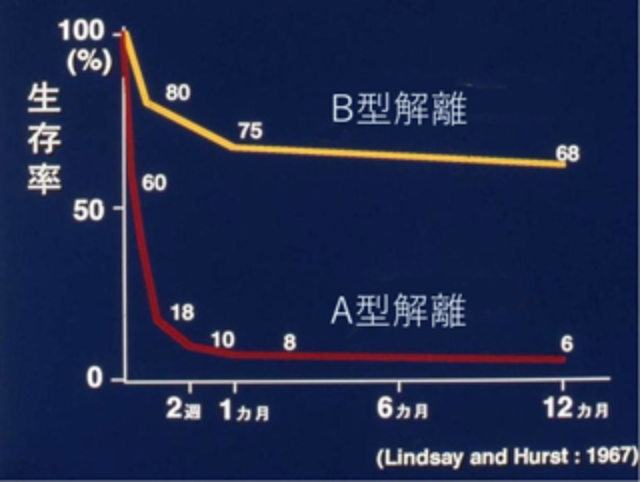
急性大動脈解離Stanford A型では先述したように約20%の患者は病院到着前に亡くなってしまします。また、無治療の場合での死亡率は最初の24時間で1時間あたり1~3%、1週間で30%、2週間で80%、1年で90%となっており、非常に予後が不良な病気の1つです。
しかし、外科治療を行うことで死亡率は減少するとの報告があり、実際に外科治療をした患者の70%は生存して退院することが出来ます。
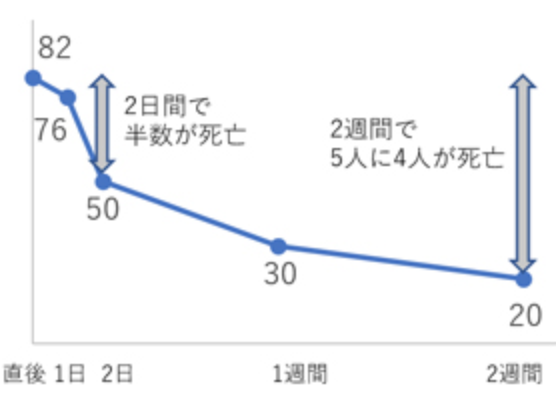
外科治療をして最初の2週間を乗り越えた場合は、5年生存率は60%、10年生存率は40%となっています。
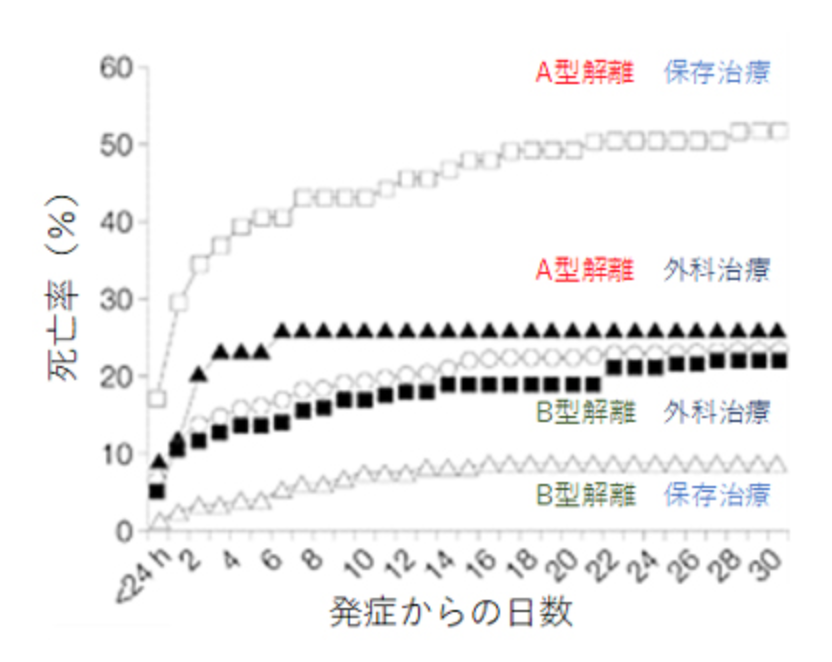
急性大動脈解離Stanford B型はA型と異なり上行大動脈に解離は進展しないため、A型と比較すると予後は良好です。合併症が無い場合は、内科治療および外科治療のどちらを選択しても、1か月後の死亡率は10%程度と報告されています。また、5年生存率は64%と報告されています。
しかし、大動脈解離発症後に偽腔が血栓閉塞するか開存しているかで予後は変化します。
Akutsu K, Nejima J, Kiuchi K et al: Effects of patent false lumen on long-term outcome of type B acute aortic dissection. Eur J Cardiothorac Surg, 2004, 26: 359–366.
そのため、急性大動脈解離Stanford B型の偽腔開存型の症例に関しては合併症がなくとも、保存的加療後三ヶ月以内にTEVARを施行することで大動脈のリモデリングが促進されます。
70歳以下の方には人工血管置換術を施行することで予後の改善が示唆されています。
大動脈瘤の予後
大動脈瘤は大きさにより破裂するリスクが異なるため、予後も異なっております。
胸部大動脈瘤の場合、年間の破裂リスクは以下のようになっております。
- 5cm未満の動脈瘤は2%
- 5~5.9cmの動脈瘤は3%
- 6cm以上の動脈瘤は8~10%
一方で、腹部大動脈瘤の場合は以下のようになっております。
- 4㎝未満の動脈瘤は0%
- 4~4.9cmの動脈瘤は1%
- 5~5.cmの動脈瘤は5~10%
- 6~6.9cmの動脈瘤は10~20%
- 7~7.9cmの動脈瘤は20~40%
- 8cm以上の動脈瘤は30~50%
風船と同じように小さいときは大きくなる速度は小さいですが、大きくなればなるほど速度も速くなります。
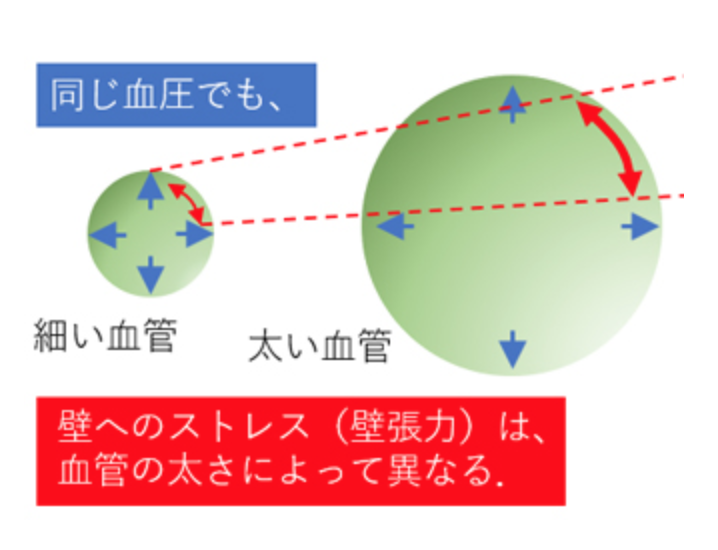
血圧が同じであっても、血管の大きさによって、壁に加わるストレスは大きく異なります。つまり血管の太さが大きくなるほど、壁には強いストレス(壁張力)が加わるのです。

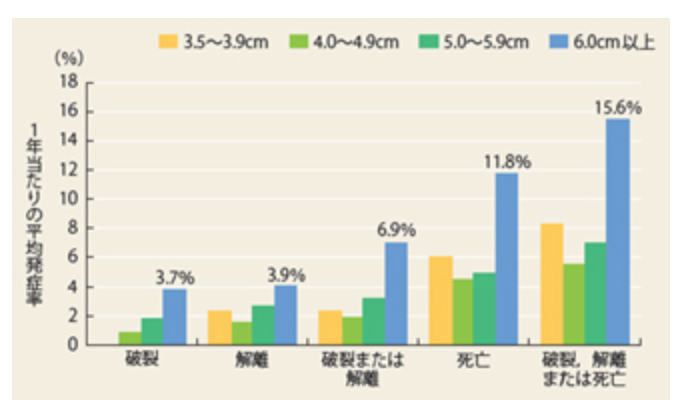
また、上の図は胸部大動脈瘤の場合、1年以内にどの程度の割合で破裂や解離、死亡といったイベントが起こるかを示しているグラフです。
大動脈瘤の大きさが6㎝を超えると約1割の方が亡くなってしまいます。 大きい胸部大動脈瘤を有する方が治療を受けない時の生存率は1年で65%,5年で20%です。このように未治療であるとかなりリスクが高いため、胸部大動脈瘤では、瘤が上行大動脈に位置する場合は5.5cm以上、下行大動脈に位置する場合は6.0cm以上、腹部大動脈瘤では5~5.5cm以上で外科治療の適応になります。
今回はこれで終わります。




コメント